同济大学左为团队与附属上海市肺科医院徐金富、瑞金医院瞿介明团队合作发表研究成果
来源:医学院
时间:2020-01-08 浏览:
呼吸道感染严重威胁人类健康。临床上针对感染的治疗主要依赖于经验性抗生素治疗,但随之而来的抗生素耐药性也引发新的临床问题。同时,肺部感染引发肺损伤、损伤进一步加重感染的恶性循环过程,则让这一问题变得更加棘手。
2020年新年伊始,同济大学附属上海市肺科医院徐金富团队、同济大学医学院左为团队以及上海交通大学医学院附属瑞金医院瞿介明团队合作,在EMBO Molecular Medicine (影响因子10.6) 上发表了题为“Genetically engineered distal airway stem cell transplantation protects mice from pulmonary infection”的研究论文(https://doi.org/10.15252/emmm.201810233)。研究团队通过构建内源性表达LL-37的改良型肺干细胞,并将其移植到小鼠肺内干预肺感染及其肺损伤后修复,该基因工程细胞具有抗感染及肺损伤的修复功能,并初步再生出兼具呼吸功能和抗菌功能的肺泡结构雏形。
研究团队首先利用LL-37转基因小鼠证实了LL-37抗菌肽能够在小鼠体内进行加工剪切,形成功能性片段。感染前后的转录组学分析表明,感染后的LL-37转基因小鼠肺部基因整体表达谱更趋向于健康小鼠。
此前同济大学医学院左为教授报道了在人类和小鼠支气管基底层存在一群Krt5+P63+远端气道干细胞(distal airway stem cell,DASC),这群细胞分布在肺部支气管的基底层位置。当机体发生大规模损伤时,这群细胞能够被诱导激活并迁移到损伤局部参与修复再生。针对此干细胞群体,左为团队开展了深入的基础研究和临床研究。依托2017年国家卫健委、药监局首批干细胞临床研究备案项目,团队实现了全球首例基于支气管基底层细胞(DASC)的肺脏再生临床试验,取得了良好的效果。
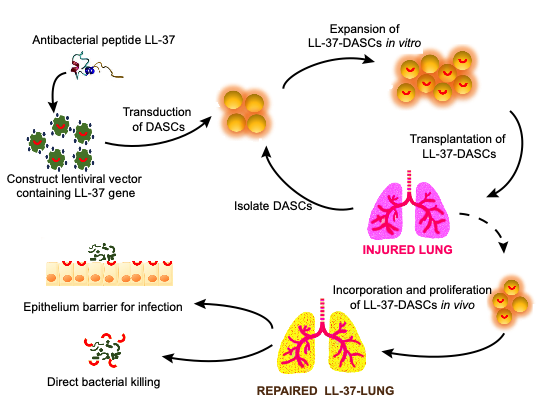
在本研究中,团队成员利用慢病毒载体将LL-37基因转入DASC中,获得能够稳定持续地表达LL-37抗菌肽的干细胞株LL-37-DASC,LL-37-DASC所释放的抗菌肽LL-37能够显著抑制细菌生长。在铜绿假单胞菌感染小鼠模型上,接受LL-37-DASC移植的肺组织能够有效地抑制细菌感染,其肺功能恢复效率远高于普通对照组小鼠。
团队从人肺中分离得到干细胞并建立内源性表达抗菌肽LL-37的干细胞系LL-37-hDASC,进而运用组织工程技术手段,将LL-37-DASC种植到脱细胞化处理的大鼠肺细胞外支架(extracellular matrix,ECM)中,初步构建了具有抗菌功能的再细胞化“人工肺”雏形。
本研究对于今后的肺干细胞再生医学临床转化具有重要意义,特别是对于肺部感染性疾病有潜在重要价值。同济大学医学院左为课题组博士生周悦青、施昀博士和同济大学附属上海市肺科医院徐金富课题组博士生杨玲为该论文共同第一作者。徐金富教授、左为教授以及瞿介明教授为论文的共同通讯作者。该研究受国家重点研发计划干细胞及转化研究专项、国家自然科学基金委、上海市人民政府、上海市申康医院发展中心、同济大学附属上海市肺科医院、同济大学附属东方医院、空军军医大学唐都医院、上海交通大学医学院附属瑞金医院、广州医科大学附属第一医院、宁夏医科大学、英国Keele University以及苏州吉美瑞生医学科技有限公司的资助。