医学院徐俊团队破解骨关节炎早期阶段慢性炎性启动软骨退变难题,创建基于工程化外泌体的骨关节炎诊疗新策略,成果发表于《骨研究》
来源:医学院
时间:2026-02-26 浏览:
全球老龄化加剧,骨关节炎(Osteoarthritis,OA)成为世界上最主要的致残性疾病之一,给社会和个人带来巨大经济负担,目前缺乏行之有效的早期诊断和治疗手段。OA是一种持续的慢性的炎症疾病,滑膜炎症发生于OA的最早期阶段,是启动和加剧关节软骨损伤的关键因素。骨髓是中枢免疫器官,是各类免疫细胞的发源地,衰老骨髓加剧全身组织衰老和功能障碍。OA发展过程中,骨髓通过血管与关节建立直接连接,促进骨髓与滑膜、软骨组织等的信号传导和细胞浸润。尽管骨髓单核/巨噬细胞(MNs)是系统性衰老的核心驱动者,但目前骨髓MNs调控OA早期慢性炎症和软骨退变的作用机制尚不明确。因此,解析上述过程的复杂调控机制,具有重大基础研究价值与转化医学意义。
2月17日,同济大学医学院、附属东方医院徐俊教授团队在《骨研究》(Bone Research)在线发表了题为“Synovial inflammatory macrophage-derived extracellular vesicles exacerbate cartilage lesions with a FMRP-selectively sorted manner in osteoarthritis”的研究成果。该研究首次证实OA早期骨髓MNs源外泌体(EVs)整合性驱动KOA病理进展:滑膜炎症、软骨退变和关节疼痛等;研发了精准靶向炎性MNs的工程化外泌体载药装置,可显著缓解临床OA样本的滑膜炎症;同时发现OA早期诊断的潜在靶点——血浆外泌体FMRP蛋白,为骨关节炎的诊疗提供新策略。

破解关键:绘制骨髓MNs调控OA早期慢性炎症和软骨退变的“外泌体功能分子图谱”和关键作用机制
临床观察已经证实,超早期滑膜炎症是加速关节软骨退变发生和发展的重要因素,同时被大量招募到炎性滑膜组织的骨髓MNs数量和功能显著发生变化。但核心科学问题长期悬而未决:骨髓MNs是否调控OA早期病理的整合性发生发展?其免疫学基础是什么?其背后的关键调控机制是什么?
为解决这一核心问题,徐俊团队系统性探索骨髓MNs整合调控OA早期病理的发生发展。研究发现,骨髓MNs源外泌体能够调节软骨细胞的自噬功能,并诱导正常关节中软骨退变的发生。从机制上讲,在OA进展过程中,骨髓MNs被大量招募到炎性滑膜组织,极化成滑膜促炎性巨噬细胞通过EVs将miR-155-5p主动转移至软骨细胞,通过抑制GSK-3β/mTORC1轴介导的自噬功能,从而加速软骨退变。在OA转基因小鼠模型中,靶向敲除骨髓MNs源miR-155可减轻软骨退变、滑膜炎症和关节疼痛,但是靶向敲除软细胞miR-155对软骨退变、滑膜炎症和关节疼痛无显著影响。另一方面,脆性X智力障碍蛋白(FMRP)选择性将miR-155-5p分选进入骨髓MNs源EVs中,且血浆EVs中FMRP的水平与OA进展密切相关,提示其可能作为OA诊断的潜在生物标志物。
临床转化:开创基于工程化外泌体的KOA诊疗新策略
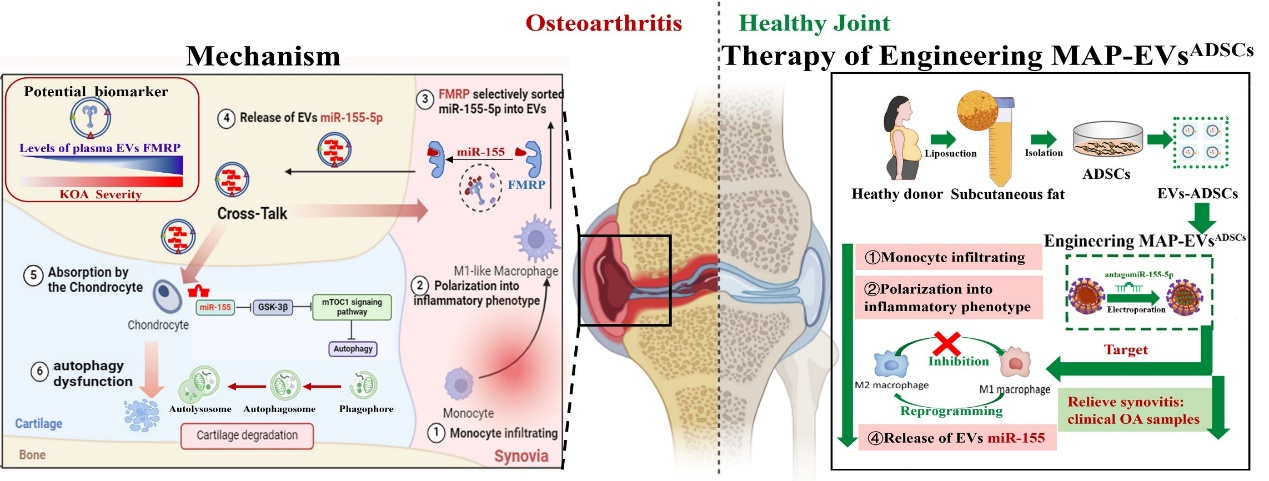
该研究的意义不仅在于揭示了OA早期骨髓MNs源外泌体(EVs)整合性驱动KOA病理进展的分子机制,证实了精准靶向炎性MNs的工程化外泌体载药装置在临床OA样本的显著功效,同时发现OA早期诊断的潜在靶点:血浆外泌体FMRP蛋白,为骨关节炎的生物医学诊疗提供全新的诊疗靶点和技术。
基于以上研究发现,干细胞外泌体介导骨关节炎诊疗的临床转化路径清晰呈现。一方面,团队借助基因编辑技术,成功构建了“靶向明确、功能增强、一靶多能”的工程化外泌体药物开发技术平台,该技术平台显著提升了骨关节炎的治疗效果,为骨关节炎的非手术治疗带来了革命性的新方案,还为慢性病管理、再生医学等相关领域的发展开辟了全新的路径。另一方面,团队正积极推进药物级别的干细胞外泌体研发,目前该项目已进入药品审评的临床前研究(preIND)阶段,已启动“干细胞外泌体治疗骨关节炎”在上海市长征医院的临床备案,快速推动临床转化研究。
同济大学医学院徐俊教授、上海交通大学附属第六人民医院杜大江主任和同济大学附属上海市第四人民医院宋建星主任为论文共同通讯作者。同济大学附属上海市第四人民医院赵姝副研究员为论文第一作者。