医学院崔磊团队揭示骨关节炎发生发展关键驱动因素为治疗提供全新靶点,成果发表于《临床研究杂志》
来源:医学院
时间:2026-03-11 浏览:
3月2日,医学院崔磊教授团队在国际权威期刊《临床研究杂志》(Journal of Clinical Investigation)在线发表题为“α-ketoglutarate protects against cartilage damage via epigenetically driven metabolic reprogramming in osteoarthritis models”的研究论文。该研究首次揭示,谷氨酰胺代谢障碍是骨关节炎发生发展的关键驱动因素,并发现其下游代谢物α-酮戊二酸(αKG)可通过表观遗传调控逆转软骨细胞的代谢失衡,为骨关节炎的治疗提供了全新靶点。

软骨细胞代谢紊乱是骨关节炎的关键驱动因素,但其背后的分子机制尚不清楚。针对这一核心科学问题,崔磊团队从临床样本切入,系统解析了骨关节炎患者及模型小鼠软骨的代谢特征。利用液相色谱-质谱联用技术,团队发现骨关节炎软骨组织中谷氨酰胺及其下游代谢物αKG水平显著下降,并与软骨损伤程度呈负相关。进一步的机制研究表明,炎症因子IL-1β通过上调组蛋白H3K27me3甲基化修饰,表观遗传沉默谷氨酰胺转运体Slc1a5及其关键酶Gls1的表达,从而抑制软骨细胞对谷氨酰胺的摄取。在体内实验中,软骨敲低Slc1a5或软骨特异性敲除Gls1均可诱导自发性骨关节炎,并加速其病程进展。
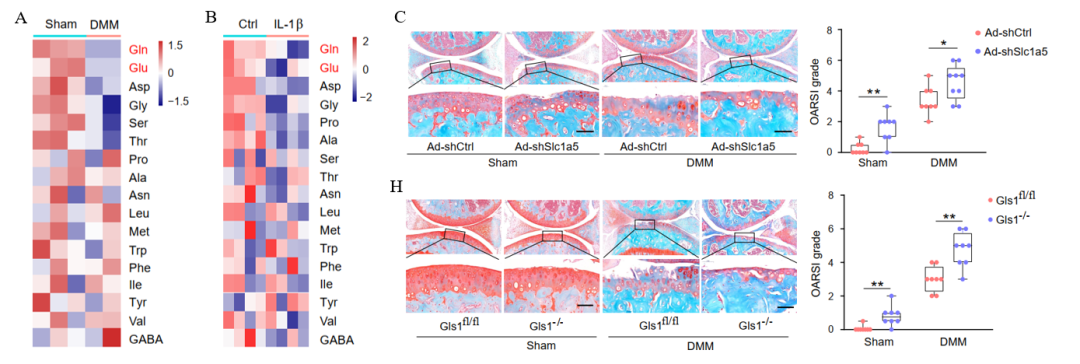
由于转运体功能受损,直接补充谷氨酰胺无法挽救软骨损伤。然而,补充其下游代谢物αKG则可有效绕过该障碍,显著恢复软骨细胞合成代谢相关基因(SOX9, COL2A1)的表达,并抑制分解代谢因子(MMP3, MMP13, ADAMTS5)的活性。在DMM诱导及肥胖相关骨关节炎小鼠模型中,关节腔注射αKG可显著延缓软骨退行性变,降低OARSI病理评分。为深入揭示αKG的软骨保护机制,研究团队综合运用单细胞测序、染色质免疫沉淀与代谢流分析等手段,发现其并非依赖传统的TCA循环或HIF-1α通路,而是作为组蛋白去甲基化酶Kdm6b的辅因子,促进H3K27me3的去甲基化。该表观遗传调控发挥“双重作用”:一方面,解除对谷氨酰胺代谢关键基因Slc1a5和Gls1的转录抑制,恢复软骨细胞对谷氨酰胺的利用;另一方面,激活Ube2o基因表达,后者通过促进TRAF6去泛素化,抑制NF-κB炎症通路,从而阻断软骨分解代谢的正反馈循环。
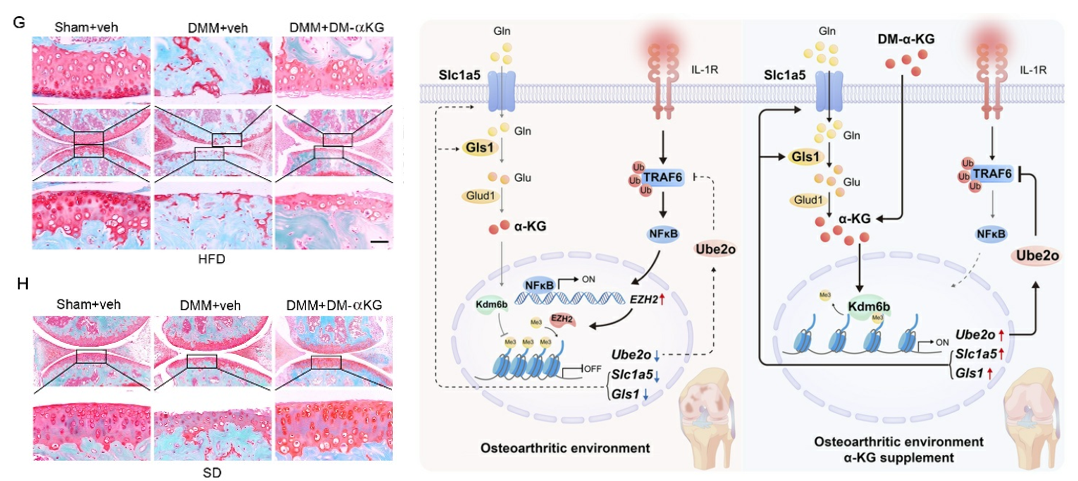
同济大学医学院、附属第十人民医院崔磊教授,医学院孙毅教授,附属东方医院尹峰教授、张昀助理研究员为论文共同通讯作者;附属第十人民医院博士后李帅军为论文独立第一作者。
论文链接:https://www.jci.org/articles/view/172380