生命科学与技术学院张儒/侯羽君团队发现RBFOX1缺失协同APOE4驱动小胶质细胞异常,揭示阿尔茨海默病新机制,成果发表于《探索》
来源:生命科学与技术学院
时间:2026-04-07 浏览:
阿尔茨海默病(AD)的发病机制复杂,APOE4作为目前已知散发性AD最强的遗传风险因子,其具体的致病调控机制尚未完全明晰。RBFOX1是一种RNA选择性剪接调控因子,虽被关联到AD易感性,但其在AD中的作用此前一直缺乏实验研究。
近日,由同济大学生命科学与技术学院张儒副教授、侯羽君教授领衔的研究团队在《探索》(Exploration)上发表了题为“RBFOX1 Dysfunction Unlocks APOE4-Associated Microglial Genesis and Exacerbates Alzheimer’s Pathology in Human Cerebral Organoids”的研究成果。该研究通过构建基因编辑的人脑类器官模型,揭示了RBFOX1与APOE4在协同诱导小胶质细胞异常及AD病理演变的深层机制,为该病的机制解析和精准干预提供了高度拟人化的研究平台。

基因编辑类器官模型发现RBFOX1缺失具有APOE4特异性效应
研究团队利用CRISPR/Cas9技术构建了APOE3或APOE4基因背景下的RBFOX1敲除人胚胎干细胞系,并进一步培育出对应的人脑类器官。实验观察到RBFOX1缺失具有明显的基因型特异性,它仅在APOE4型人脑类器官中特异性诱导出小胶质细胞,而在APOE3型类器官中则未观察到此现象。这些自发生长的小胶质细胞比例与人类大脑中小胶质细胞占比(5%-15%)相近,克服了传统人脑类器官诱导途径缺乏内源性小胶质细胞的局限。进一步研究表明,这种APOE4特异性的小胶质细胞生成,与类器官早期胚状体分化阶段中胚层启动时间的持续延长密切相关。具体而言,TGFβ/WNT信号通路的异常激活为小胶质细胞谱系分化创造了条件,而恢复RBFOX1表达可逆转该信号通路的异常,证实了RBFOX1在调节人类中胚层发育和小胶质细胞生成的重要作用。
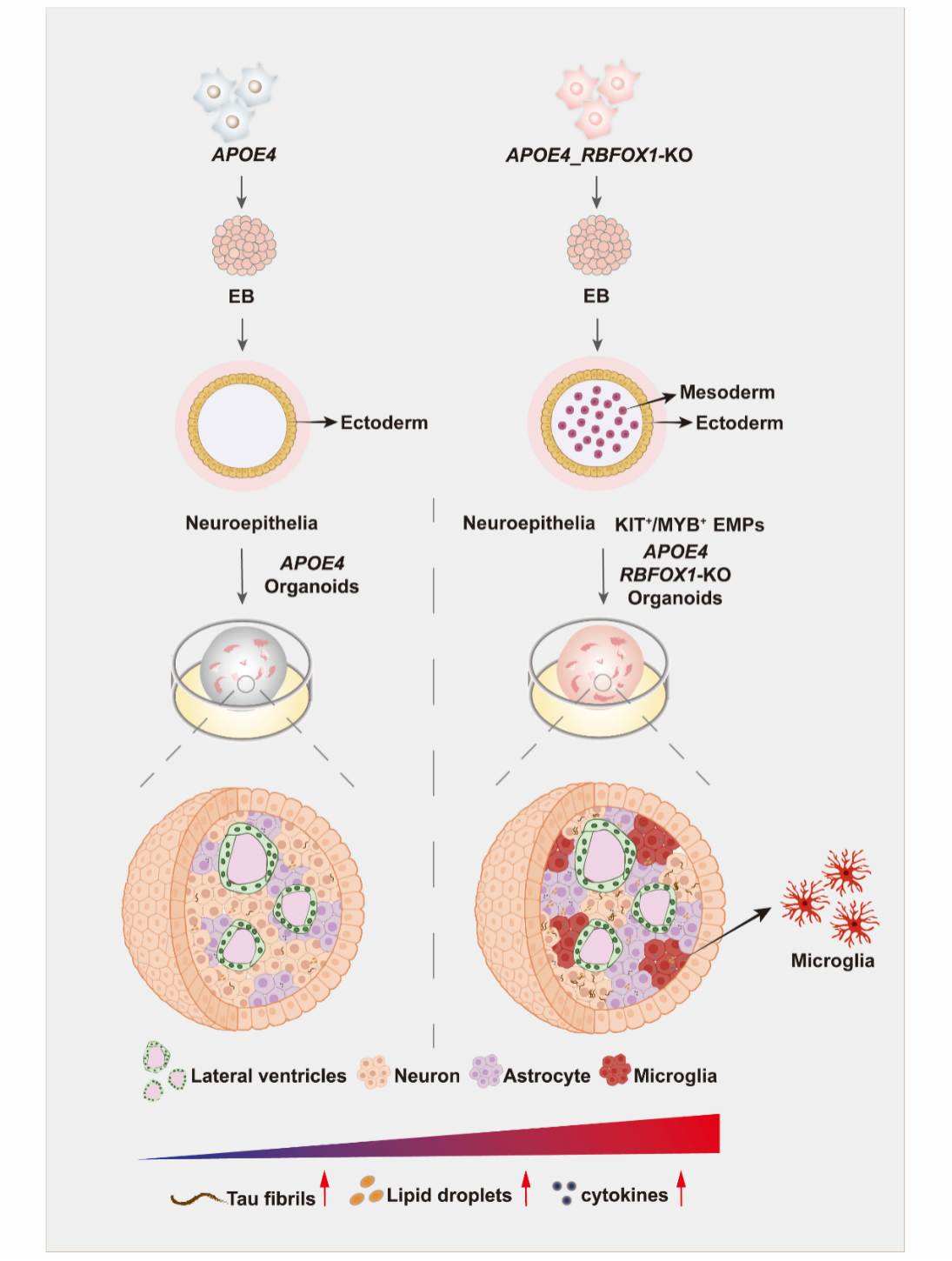
异常小胶质细胞引发多重AD病理损伤,构建多维度AD病理模型
研究进一步发现,RBFOX1缺失诱导的APOE4型类器官小胶质细胞呈现出明显的神经毒性表型:不仅大量分泌促炎因子,引发强烈的神经炎症反应,还伴随脂滴异常积累,破坏脂质代谢稳态;同时,这些异常小胶质细胞还会导致突触结构重塑,并与过度磷酸化的Tau蛋白共定位,加剧APOE4型类器官的Tau病理损伤,而对Aβ沉积无明显影响,揭示了RBFOX1在AD中对Tau病理的特异性调控作用。电生理检测进一步证实,APOE4型RBFOX1敲除类脑器官的神经元网络功能出现显著异常,包括棘波、爆发次数及平均放电率均明显降低,较好地模拟了AD患者的神经元功能障碍特征。
该模型首次在人脑类器官构建中实现了内源性小胶质细胞的自主形成,并整合了神经炎症、Tau过度磷酸化、脂质代谢紊乱、突触重塑和神经元网络功能异常等多重AD核心病理特征,成为研究AD基因型依赖性神经元-胶质细胞相互作用的理想平台。
定位RBFOX1为AD保护性因子,为精准治疗提供新方向
这项研究明确了RBFOX1作为AD潜在保护因子的角色,作为APOE4-胶质细胞相互作用的关键抑制因子,其功能缺失会释放出小胶质细胞介导的神经退行性级联反应,与APOE4协同加剧AD病理损伤。这一发现为理解散发性AD的多基因调控机制提供了新的深度。
此外,该研究构建的具有自主生成小胶质细胞网络的APOE4型RBFOX1敲除人脑类器官模型,突破了传统人脑类器官构建过程中缺乏小胶质细胞的局限性,为解析AD中基因型特异性的神经-胶质相互作用、筛选靶向小胶质细胞的AD治疗药物提供了更贴近生理状态的研究工具,具有重要的转化医学潜力。
同济大学生命科学与技术学院张儒副教授、侯羽君教授为论文共同通讯作者,团队成员张博文博士为论文第一作者。该研究得到了脑科学与类脑研究国家科技重大专项、国家自然科学基金、上海市自然科学基金等支持。
论文链接:https://doi.org/10.1002/exp2.70160