生命科学与技术学院李维达/晏家骢等合作提出一种用于优化干细胞来源胰岛类器官移植效果的新型预处理策略,成果发表于《细胞·干细胞》
来源:生命科学与技术学院
时间:2026-04-03 浏览:
4月2日,同济大学李维达教授团队与云南省第一人民医院晏家骢研究员团队在《细胞·干细胞》(Cell Stem Cell)上发表研究论文,提出了一种用于优化干细胞来源胰岛类器官(SC-islets)移植效果的新型预处理策略。
该策略主要针对SC-islets临床转化过程中移植早期与后期面临的两类关键问题:一是在移植初期的急性缺血缺氧阶段,超过50%的移植物会因缺氧等因素死亡;二是在后续的慢性高血糖损伤阶段,存活下来的β细胞又容易发生身份丢失,功能逐渐衰退。在该研究中,则重点针对移植早期缺血缺氧这一核心瓶颈,通过移植前的小分子预处理,使SC-islets获得多重适应能力,从而同时提升其早期存活率及后期功能稳定性。
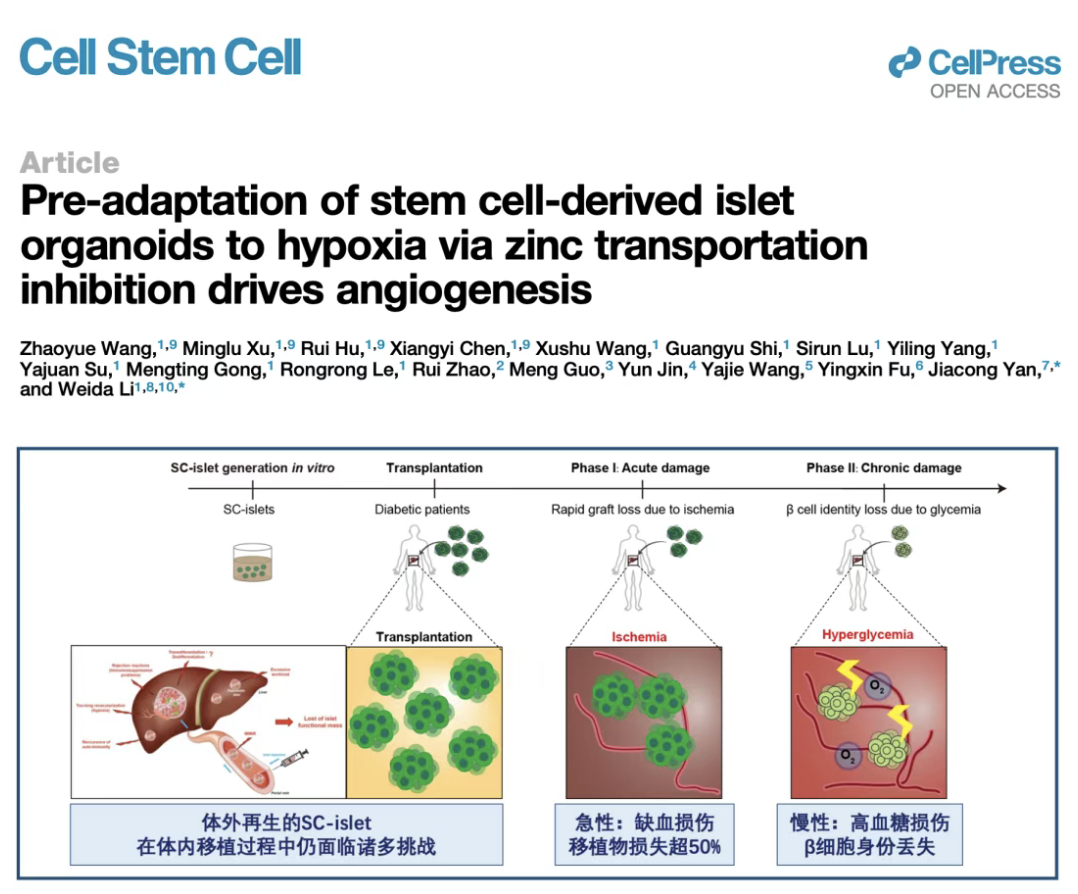
SC-islets移植面对的两个“劫”:急性缺血损伤和慢性高血糖损伤
早先的人类遗传学研究发现,锌转运蛋白ZnT8的功能缺失突变与2型糖尿病风险显著降低有关。李维达团队随后在Nature Communications、Advanced Science、Cell Research期刊上揭示了ZnT8介导的锌离子异常积累在胰岛β细胞功能衰竭中的关键角色,并基于此开发了全球首个靶向ZnT8的小分子抑制剂,解决了上述慢性高血糖损伤的问题。
在最新工作中,团队将目光投向了更具挑战性的源头,即如何制造出“更强壮”的胰岛类器官。他们发现,在干细胞分化而来的胰岛类器官中,β细胞内的锌离子水平异常升高。过量的锌会诱发活性氧堆积,导致细胞能量代谢的核心调控蛋白AMPK发生氧化修饰并失活,这使得细胞难以应对移植后的恶劣环境,包括低氧和缺乏血管化。
研究的关键在于,使用团队筛选获得的ZnT8小分子抑制剂对胰岛类器官进行预处理,能够有效纠正锌离子积累,重新激活AMPK。这相当于在移植前为细胞完成了一次全面的耐逆性升级。激活的AMPK如同一道总开关,赋予了细胞三大特性:功能成熟,使其胰岛素分泌能力显著增强;低氧耐受,增强其在缺血环境下的存活能力;促进血管化,尤为重要的是,研究发现AMPK能通过新路径直接上调血管内皮生长因子的表达,驱动血管快速向移植物生长,并且维持长期功能。
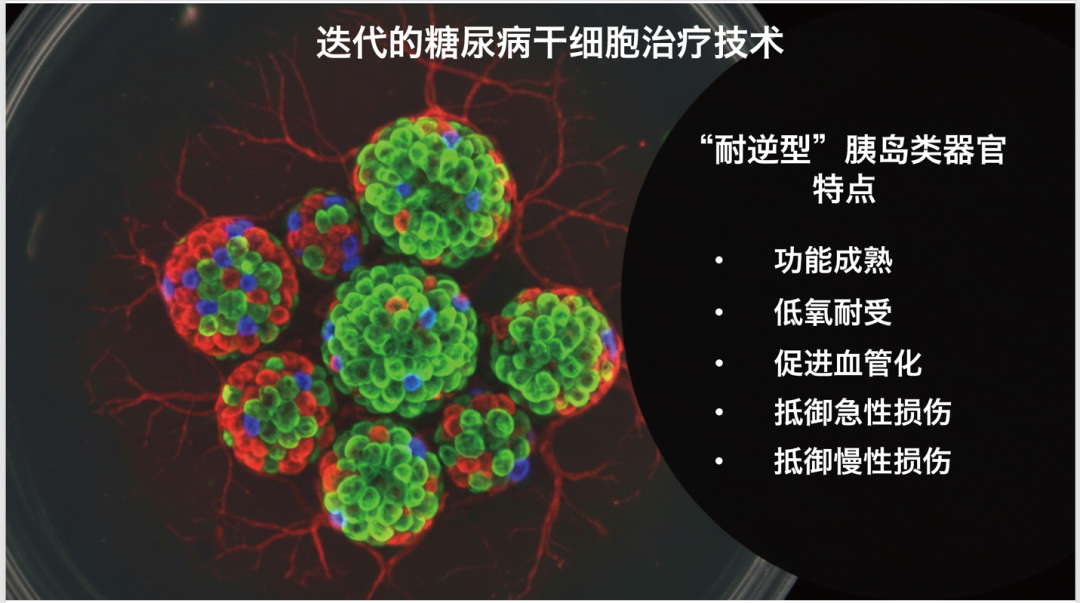
“耐逆型”胰岛类器官特点
综上,李维达教授团队和晏家骢研究员团队开发的“耐逆型”胰岛类器官的技术,实现了从“抵御急性损伤”到“防止慢性衰竭”的系统性防护,是糖尿病干细胞治疗技术的一次重要迭代。目前,这项从靶点发现、机制解析到产品开发的系统性创新,已步入临床转化阶段。李维达团队正与云南省第一人民医院开展紧密合作,共同推进基于该“耐逆型”胰岛类器官的临床研究,致力于将这项有望实现“一次移植、长期有效”的变革性疗法,早日推向临床应用。
同济大学生命科学与技术学院博士研究生王昭月、博士研究生许明璐、博士后胡瑞,博士研究生陈相宜为论文共同第一作者。同济大学生命科学与技术学院李维达教授、云南省第一人民医院晏家骢研究员为共同通讯作者。云南省第一人民医院晋云主任、王娅婕主任,深圳市第三人民医院付迎欣主任、海军军医大学郭猛教授也对该研究有重要贡献。
论文链接:https://doi.org/10.1016/j.stem.2026.03.004