生命科学与技术学院杨静团队联合研究发现靶向清除CAR-Tregs,天然产物TAIII让CAR-T疗法“如虎添翼”,成果发表于《自然·通讯》
来源:生命科学与技术学院
时间:2026-04-01 浏览:
CAR-T疗法虽然改变了血液肿瘤的治疗格局,但半数患者仍会面临耐药与复发。临床研究发现,一个“潜伏的敌人”正在暗中破坏疗效——CAR-调节性T细胞(CAR-Tregs)。这些细胞在CAR-T产品中占比虽小,却能强力抑制“主力部队”CAR-T效应细胞的功能,成为治疗失败的关键推手。如何在不伤及效应细胞的前提下精准清除CAR-Tregs,是突破疗效瓶颈的核心难题。
3月31日,同济大学生命科学与技术学院杨静研究员、附属同济医院梁爱斌教授,联合中国科学院合肥物质科学研究院刘青松研究员团队在《自然·通讯》(Nature Communications)上发表题为“Timosaponin AIII enhances CAR-T cell potency and prevents relapse through impairing CAR-Tregs”的研究成果,首次发现源自中药知母的天然产物知母皂苷AIII(TAIII)能够精准清除CAR-Tregs、显著增强CAR-T疗法的抗肿瘤效果并防止复发。

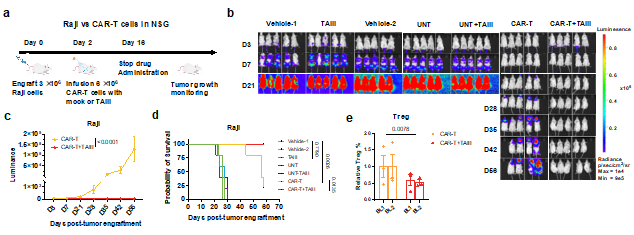
研究团队首创基于Treg-IL-2调控功能的高通量筛选系统,从3000余种天然产物及已上市药物中成功锁定TAIII。这一源自传统中药的甾体皂苷分子,展现出强大的Treg抑制能力和优异的安全性,更令人惊喜的是——它已作为抗皱剂完成临床试验,安全性已获验证,临床转化路径清晰。机制研究揭示,TAIII是一位精准的“狙击手”。它别构结合于A2A腺苷受体(A2AR)的胆固醇结合口袋,竞争性置换胆固醇,从而阻断A2AR下游的cAMP-PKA-CREB信号通路。这一作用直击Tregs的“命门”——转录因子FoxP3,从源头上削弱CAR-Tregs的抑制功能。当A2AR被敲除或Tregs被清除后,TAIII的增效作用完全消失,特异性毋庸置疑。TAIII处理使CAR-T产品中Treg比例下降约40%,同时促进更具长效潜力的中央记忆型T细胞(Tcm)形成。这意味着可以在体外“优化”CAR-T产品,从源头上提升疗效。在多种白血病/淋巴瘤小鼠模型中,TAIII联合给药或仅对CAR-T细胞进行短期预处理,均能显著增强肿瘤清除能力、有效防止复发、大幅延长生存期。在更具挑战的实体瘤模型中,TAIII不仅显著增敏CAR-T细胞疗法,更能与PD-1抗体协同增效,系统性重塑肿瘤微环境,将免疫抑制的“冷”肿瘤逆转为CD8+T浸润的“热”肿瘤。从临床复发患者体内收集的CAR-T细胞,在TAIII处理后杀伤活性被显著“唤醒”,效应细胞因子分泌恢复。这意味着TAIII有望成为挽救CAR-T无应答或复发患者的“后手棋”。TAIII的应用场景极为灵活:既可成为CAR-T制备过程中的“添加剂”,在体外优化细胞产品;也可作为体内联合治疗的“增效剂”,与CAR-T或免疫检查点抑制剂联用。特别是对于生产批次不佳、Treg比例过高的CAR-T产品,TAIII预处理可能成为一种行之有效的质控手段。
该研究不仅首次揭示TAIII作为A2AR别构抑制剂清除CAR-Tregs的新机制,更完成了从靶点发现、机制解析到临床验证的完整闭环。与现有策略相比,TAIII实现了对Tregs的精准清除,同时保留并增强效应细胞功能,真正做到了“扬清激浊”。基于TAIII已通过临床试验的安全性验证,其向肿瘤免疫治疗临床应用的转化路径已豁然开朗。这一源自中药宝库的“黄金分子”,有望成为CAR-T疗法中不可或缺的“黄金搭档”,帮助更多患者实现持久深度缓解,迈向治愈。
同济大学生命科学与技术学院杨静研究员、附属同济医院梁爱斌教授,中国科学院合肥物质科学研究院刘青松教授为论文共同通讯作者。中国科学院合肥物质科学研究院博士生侯明琪、副研究员齐紫平,附属同济医院张文君主任、生命科学与技术学院博士生李桂明为论文共同第一作者。该研究获国家自然科学基金、国家重点研发计划等支持。
论文链接:https://doi.org/10.1038/s41467-026-70867-5